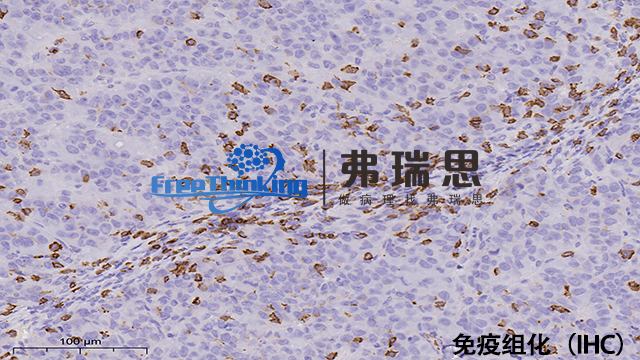
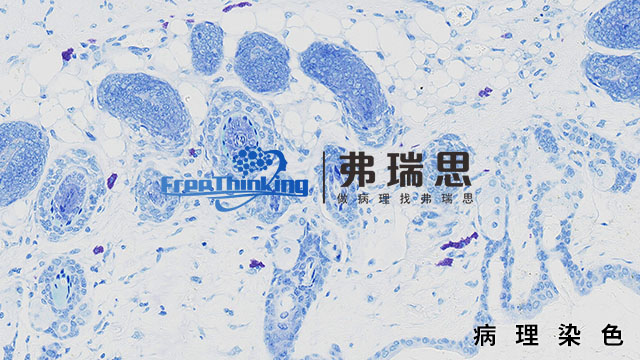
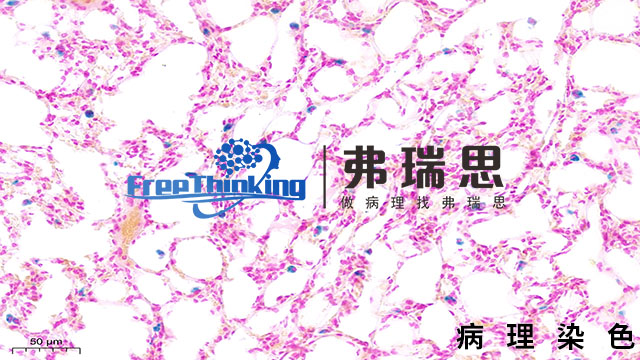
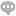免疫组化研究细胞周期蛋白与凋亡蛋白变化的关键步骤如下:首先,组织样本处理。对样本进行固定、切片等操作,确保样本结构完整且适合后续实验。其次,选择特异性抗体。针对细胞周期蛋白和凋亡蛋白分别挑选高特异性的抗体。然后,进行抗体孵育。优化抗体浓度、孵育时间和温度等条件,使抗体与目标蛋白充分结合。接着,显色反应。加入相应的显色剂,使结合抗体的蛋白在组织中呈现出可观察的颜色变化。之后,图像采集。使用显微镜采集染色后的组织图像,注意图像的清晰度和分辨率。之后,图像分析。通过分析软件测量蛋白表达的强度、分布等指标,从而推断细胞周期蛋白与凋亡蛋白的变化情况,为进一步研究提供依据。免疫组化是否可以助力制定更合理的治疗方案呢?北京病理切片免疫组化扫描
在免疫组化实验中,切片厚度主要在以下方面影响实验结果。一方面,较薄的切片有利于抗原抗体充分结合。切片薄能使抗体更易渗透到组织内部,与抗原接触更充分,提高染色的均匀性和特异性,减少背景染色,使结果更清晰准确。另一方面,过薄的切片可能在操作中易破碎,增加实验难度。而较厚的切片可能导致抗体渗透不充分,出现染色不均,且可能掩盖部分细微结构,影响对目标抗原的定位和观察。同时,厚切片可能增加非特异性结合的机会,使背景染色增强,降低实验结果的准确性和特异性。合适的切片厚度需根据组织类型和实验目的进行调整。北京病理切片免疫组化扫描免疫组化中的抗原修复方法多样,如热修复、酶消化法等,目的是暴露被掩盖的抗原表位。
在荧光共定位研究的免疫组化实验中,选择荧光标记抗体有以下关键策略:一是合理选择荧光染料。要考虑不同荧光染料的激发和发射光谱,尽量选择光谱重叠少的染料进行多色标记,以清晰区分不同的目标抗原。二是优化抗体浓度。通过预实验来确定合适的荧光标记抗体浓度,既能保证足够的信号强度,又可避免非特异性结合产生的背景干扰。三是注意样本处理。确保样本的固定和通透处理方式适合荧光标记抗体的结合,保证抗原的完整性和可及性。四是做好对照实验。设置阳性对照和阴性对照,阳性对照用于验证抗体的有效性,阴性对照可排除非特异性结合等因素的干扰。
免疫组化即免疫组织化学技术。它是利用抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂显色来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及相对定量的研究。首先将组织样本进行处理,如固定、切片等。然后利用特定的抗体与组织中的目标抗原结合,再通过带有标记的二抗与一抗结合,使目标抗原被标记上可检测的物质,如荧光素或酶等。在显微镜下观察组织中抗原的分布和表达情况。免疫组化技术在病理诊断、生物学研究等领域有着广泛应用,可帮助判断疾病的类型、进展程度,研究细胞的功能和分子机制等。组织微阵列结合免疫组化可高通量分析临床样本蛋白表达。
免疫组化具有以下特点:一、特异性强1.利用抗原与抗体的特异性结合,能准确识别特定的生物分子在组织或细胞中的位置。不同的抗体针对不同的抗原,可实现对特定蛋白等物质的准确定位,减少非特异性染色带来的干扰。二、定位准确1.可以清晰地显示目标分子在细胞内的具体分布,如细胞核、细胞质或细胞膜等部位。有助于深入了解生物分子在细胞中的作用位置及与其他细胞结构的关系。三、灵敏度高1.能够检测出低丰度的生物分子。即使目标分子在组织或细胞中的含量极少,通过合适的抗体和显色方法,也能被有效地检测出来,为研究微量分子的生物学意义提供可能。四、结合形态学观察1.将分子水平的检测与组织或细胞的形态学观察相结合。在观察组织或细胞的结构形态同时,了解特定生物分子的表达情况,为疾病诊断和研究提供更准确的信息。定量分析软件可对免疫组化结果进行半定量评估。北京病理切片免疫组化扫描
免疫组化利用抗原抗体反应定位组织中的特定蛋白。北京病理切片免疫组化扫描
在免疫组化实验中,可通过以下方式减少背景染色。一是优化抗体浓度,浓度过高可能导致非特异性结合增加,产生背景染色,所以要根据实验摸索出合适的抗体浓度。二是充分洗涤,在每一步反应后进行充分的洗涤,比如使用合适的缓冲液多次冲洗,去除未结合的抗体和其他杂质。三是对样本进行合理处理,例如适当调整固定剂的种类、固定时间和固定温度,减少因固定不当而导致的抗原暴露过度引起的非特异性结合。四是使用封闭剂,选择合适的封闭液,如正常血清等,在加入抗体前进行封闭,可减少抗体与样本中其他蛋白的非特异性结合。北京病理切片免疫组化扫描
文章来源地址: http://swfw.spyljgsb.chanpin818.com/yiliaofuwu/deta_27627008.html
免责声明: 本页面所展现的信息及其他相关推荐信息,均来源于其对应的用户,本网对此不承担任何保证责任。如涉及作品内容、 版权和其他问题,请及时与本网联系,我们将核实后进行删除,本网站对此声明具有最终解释权。



 [VIP第1年] 指数:3
[VIP第1年] 指数:3